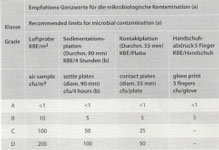
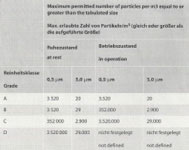
GMP (EU – GMP – Leitfaden) / FDA – RLT – Reinräume
Herstellung steriler Arzneimittel:
- Design Qualification (DQ) - Designqualifizierung
Die DQ ist der dokumentierte Nachweis, dass die Anlagen den Vorgaben des GMP-Leitfadens und dem Stand der
Technik entspricht.
- Installation Qualification (IQ) - Installationsqualifizierung
Die IQ ist der dokumentierte Nachweis, dass die Anlage gemäß der DQ installiert wurde und alle für den Prozess
relevanten Komponenten entsprechend den Zertifikaten und evtl. Festlegungen bei durchgeführten Werk-Audits
installiert wurde.
- Operation Qualification (OQ) - Funktionsqualifizierung
Die OQ ist der dokumentierte Nachweis, dass die Anlage alle geplanten und in der DQ spezifizierten Funktionen erfüllt. Es wird nachgewiesen, dass alle prozessbedingten Parameter erreicht werden. Die Art der Prüfungen wird in der OQ
beschrieben und daraus resultierende Prüfprotokolle werden der OQ beigefügt.
- Performance Qualification (PQ) - Leistungsqualifizierung
Die PQ ist der dokumentierte Nachweis, dass die Anlage eine erfolgreiche und reproduzierbare Produktion gemäß den
spezifizierten Leistungen erbringt.
Reinraumtechnik/Reinraumwartung/Reinraummesstechnik/Reinraumqualifizierung